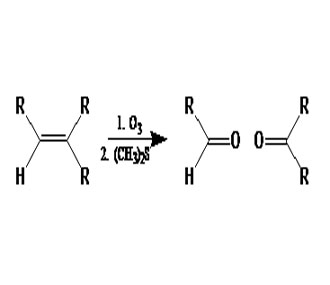
臭氧分解是一種利用臭氧裂解不飽和有機鍵的過程。臭氧不會在飽和碳中心發生反應,而是以2 + 3協同方式在不飽和體系中以1,3-偶極加成反應��,這使得臭氧在有機化學中具有實用性�����。
臭氧分解機制很早由Rudolf Criegee于1953年提出����。
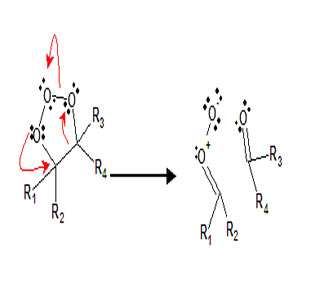
臭氧分解機制如下所示:
臭氧與烯烴在1,3-偶極環加成反應中與molozonide(也稱為主要臭氧化物)反應,其是具有3個相鄰氧原子(1,2,3-三氧雜環戊烷)的5元環結構����。該中間體是不穩定的并且在環化反應中開放以形成兩性離子和羰基化合物�,通常稱為“Criegee Intermediate”���。在第三個反應步驟中����,羰基化合物和兩性離子在另一個環加成反應中形成二級臭氧化物�,其也是五元環,但具有2個相鄰的氧原子(過氧化物鍵),第三個插入原始碳碳雙鍵中作為醚鍵(1,2,4-三氧雜環戊烷)。在同位素標記中發現了這種機制的證據��。用17O(氧-17)標記的苯甲醛在臭氧分解反應中與兩性離子中間體反應���,同位素僅在臭氧化物的醚鍵中結束[1]�。注意,如果碳鏈雙鍵位于鏈的末端,即R1-CH = CH2���,則會形成二氧化碳(CO2)。臭氧分解的實用方面壬二酸和壬酸是由油酸的臭氧分解產生的。 。用17O(氧-17)標記的苯甲醛在臭氧分解反應中與兩性離子中間體反應�����,同位素僅在臭氧化物的醚鍵中結束[1]����。注意,如果碳鏈雙鍵位于鏈的末端,即R1-CH = CH2��,則會形成二氧化碳(CO2)�。臭氧分解的實用方面壬二酸和壬酸是由油酸的臭氧分解產生的。 。用17O(氧-17)標記的苯甲醛在臭氧分解反應中與兩性離子中間體反應���,同位素僅在臭氧化物的醚鍵中結束[1]。注意,如果碳鏈雙鍵位于鏈的末端,即R1-CH = CH2,則會形成二氧化碳(CO2)���。臭氧分解的實用方面壬二酸和壬酸是由油酸的臭氧分解產生的。 。
如何使用臭氧分解獲得很佳效果
高臭氧濃度可以很有效地進行臭氧分解反應���。臭氧濃度高于10%可獲得優異的結果; 但是,臭氧濃度越高,結果越好����??焖俎D化很重要�����,因為通常處理的樣品非常小(在100-250毫升之間)�。較小的樣品比較大的樣品干燥得更快����,因為進入樣品的氣體(臭氧和氧氣)非常干燥���。